Genetik bozuklukların tedavisinde yeni bir seçenek: Gen optimizasyonu
 Spesifik yüzey belirteçleri aracılığıyla farklı hedef hücrelere kontrollü gen transferi mevcut diğer yöntemlere göre daha etkili bulundu. Yeni yöntemle hedef hücrelere gen transferi, ilave toksisite olmaksızın yapılabiliyor. Genetik bilginin lentiviral transfer kullanılarak gerçekleştirilen gen terapileri böylece optimize edilebilir. Biomaterials Dergisi’nde yayımlanan çalışmaya göre, Retrovirüs ailesine ait Lentivirüsler, hücrelerdeki genetik materyali değiştirmek için vektör olarak kullanılabiliyor ve gen terapisi tarafından belirlenen kusurlu bir genin değiştirilmesi için ciddi bir yöntem haline gelebilir. Bu tip bir tedavinin etkililiğini artırmak, majör bir tıbbi güçlük ortaya çıkarmaktadır: Virüs spesifik olarak hedef hücreyi izlemelidir ve kullanılan virüs sayısı mümkün olduğu kadar düşük olmalıdır.
Spesifik yüzey belirteçleri aracılığıyla farklı hedef hücrelere kontrollü gen transferi mevcut diğer yöntemlere göre daha etkili bulundu. Yeni yöntemle hedef hücrelere gen transferi, ilave toksisite olmaksızın yapılabiliyor. Genetik bilginin lentiviral transfer kullanılarak gerçekleştirilen gen terapileri böylece optimize edilebilir. Biomaterials Dergisi’nde yayımlanan çalışmaya göre, Retrovirüs ailesine ait Lentivirüsler, hücrelerdeki genetik materyali değiştirmek için vektör olarak kullanılabiliyor ve gen terapisi tarafından belirlenen kusurlu bir genin değiştirilmesi için ciddi bir yöntem haline gelebilir. Bu tip bir tedavinin etkililiğini artırmak, majör bir tıbbi güçlük ortaya çıkarmaktadır: Virüs spesifik olarak hedef hücreyi izlemelidir ve kullanılan virüs sayısı mümkün olduğu kadar düşük olmalıdır.
 Fraunhofer Enstitüsü ve Münih’teki Radyasyon Biyolojisi Enstitüsü’nden Dr. Ines Höfig tarafından yönetilen bir araştırma ekibi, virüs transdüksiyonunun etkisini artıran bir adjuvan geliştirdi. Böylece hedef hücrelere transfer, ilave toksisite olmaksızın optimize edilmiş oldu. Çalışmadan elde edilen bulguların gen transferi ve hasarlı genlerden kaynaklanan hastalıkların tedavisinde önemli bir gelişme sağlayacağı belirtiliyor.
Fraunhofer Enstitüsü ve Münih’teki Radyasyon Biyolojisi Enstitüsü’nden Dr. Ines Höfig tarafından yönetilen bir araştırma ekibi, virüs transdüksiyonunun etkisini artıran bir adjuvan geliştirdi. Böylece hedef hücrelere transfer, ilave toksisite olmaksızın optimize edilmiş oldu. Çalışmadan elde edilen bulguların gen transferi ve hasarlı genlerden kaynaklanan hastalıkların tedavisinde önemli bir gelişme sağlayacağı belirtiliyor.
Yüzey molekülleri virüsleri hedef hücrelerle birleştirir
Bilim insanları virüsleri, virüslerin hedef hücrelerine tutunmasını kolaylaştıran ilave yüzey molekülleriyle donattı. Yüzey molekülleri, bir antikor fragmanıyla birleşen glikoproteinlerden oluşmaktadır. Bu antikor fragmanı, EGFR+ veya CD30+ gibi, spesifik hedef hücrelerin yüzey reseptörlerini tespit eder ve bunlara bağlanır.
Yüksek transdüksiyon oranı – daha az virüs kullanımı
Araştırma grubu lideri Dr. Ines Höfig, yürüttükleri çalışma ile ilgili şu bilgileri veriyor: “Hedef hücrelere bu spesifik bağlanmayla, transdüksiyon oranını (virüslerin hedef hücrelere transferini) üç kat artırabiliriz. Böylece, trasndüksiyon etkililiği artırılır ve aynı zamanda daha az transfer virüsüne ihtiyaç duyulur.”
 Daha ileri çalışmalarda, yerleşik sisteme benzer, uygun antikor fragmanları çeşitli hedef hücrelerin, örn. kemik iliği kök hücreleri ve immün hücrelerin, spesifik yüzey belirteçleri için değerlendirilmelidir. Gen terapisi böylece spesifik genetik bozuklukların (örn. metakromatik lökodistrofi, Wiskott-Aldrich sendromu) tedavisi olarak kullanılabilir.
Daha ileri çalışmalarda, yerleşik sisteme benzer, uygun antikor fragmanları çeşitli hedef hücrelerin, örn. kemik iliği kök hücreleri ve immün hücrelerin, spesifik yüzey belirteçleri için değerlendirilmelidir. Gen terapisi böylece spesifik genetik bozuklukların (örn. metakromatik lökodistrofi, Wiskott-Aldrich sendromu) tedavisi olarak kullanılabilir.
Makalenin tam metnine aşağıdaki linkten ulaşılabilir:
http://www.ncbi.nlm.nih.gov/pubmed/24529898
Abstract
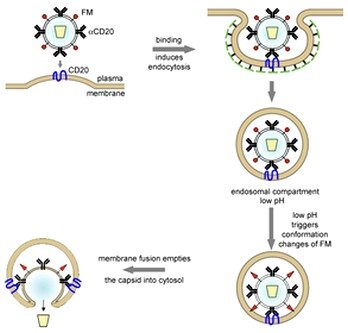 Lentiviral vectors (LV) are widely used to successfully transduce cells for research and clinical applications. Lentiviral vectors pseudotyped with the vesicular stomatitis virus glycoprotein (VSV-G) can be produced to high titers and mediate high transduction efficiencies in vitro. For clinical applications the need for optimized transduction protocols and the limited activity of retronectin as LV enhancer, results in the application of a high multiplicity of infection (MOI) to achieve effective transduction efficiencies for a number of therapeutically relevant cells, e.g. CD34(+) hematopoietic stem cells, T- and B-cells. Our study describes an optimized LV infection protocol including a non-toxic poloxamer-based adjuvant combined with antibody-retargeted lentiviral particles, improving transduction efficiency at low MOI. Cell specificity of lentiviral vectors was increased by displaying different ratios of scFv-fused VSV-G glycoproteins on the viral envelope. The system was validated with difficult to transduce human CD30(+) lymphoma cells, and EGFR(+) tumor cells. Highly efficient transduction of lymphoma cells was achieved, >50% of cells were transduced when MOI 1 was used. The scFv displaying lentiviral particles gained relative specificity for transduction of target cells. Preferential gene delivery to CD30(+) or EGFR(+) cells was increased 4-fold in mixed cell cultures by presenting scFv antibody fragments binding to respective surface markers. A combination of spinoculation, poloxamer-based chemical adjuvant, and LV displaying scFv fragments increases transduction efficiencies of hard-to-transduce suspension lymphoma cells, and promises new chances for the future development of improved clinical protocols.
Lentiviral vectors (LV) are widely used to successfully transduce cells for research and clinical applications. Lentiviral vectors pseudotyped with the vesicular stomatitis virus glycoprotein (VSV-G) can be produced to high titers and mediate high transduction efficiencies in vitro. For clinical applications the need for optimized transduction protocols and the limited activity of retronectin as LV enhancer, results in the application of a high multiplicity of infection (MOI) to achieve effective transduction efficiencies for a number of therapeutically relevant cells, e.g. CD34(+) hematopoietic stem cells, T- and B-cells. Our study describes an optimized LV infection protocol including a non-toxic poloxamer-based adjuvant combined with antibody-retargeted lentiviral particles, improving transduction efficiency at low MOI. Cell specificity of lentiviral vectors was increased by displaying different ratios of scFv-fused VSV-G glycoproteins on the viral envelope. The system was validated with difficult to transduce human CD30(+) lymphoma cells, and EGFR(+) tumor cells. Highly efficient transduction of lymphoma cells was achieved, >50% of cells were transduced when MOI 1 was used. The scFv displaying lentiviral particles gained relative specificity for transduction of target cells. Preferential gene delivery to CD30(+) or EGFR(+) cells was increased 4-fold in mixed cell cultures by presenting scFv antibody fragments binding to respective surface markers. A combination of spinoculation, poloxamer-based chemical adjuvant, and LV displaying scFv fragments increases transduction efficiencies of hard-to-transduce suspension lymphoma cells, and promises new chances for the future development of improved clinical protocols.
YAZIYI PAYLAŞ


 Gen terapisiyle HIV’e karşı uygulanan kalkan başarılı sonuç verdi
Gen terapisiyle HIV’e karşı uygulanan kalkan başarılı sonuç verdi Kalp hücreleri gen enjeksiyonuyla ‘Biyolojik Pacemaker’a dönüştürüldü!
Kalp hücreleri gen enjeksiyonuyla ‘Biyolojik Pacemaker’a dönüştürüldü! Kanser tedavisinde immün yanıtı tetikleyen yeni bir aşı!
Kanser tedavisinde immün yanıtı tetikleyen yeni bir aşı! Yeni kanser aşısı pek çok tümör tipinde etkili sonuçlar verdi!
Yeni kanser aşısı pek çok tümör tipinde etkili sonuçlar verdi! Kanser tedavisinde gen modifikasyonu, FDA’nın onayladığı ilk genetik terapi oldu
Kanser tedavisinde gen modifikasyonu, FDA’nın onayladığı ilk genetik terapi oldu
YORUMUNUZ VAR MI?