The Lancet: Rus Sputnik V aşısının yapıldığı gönüllülerde antikor gelişti
Rus Covid-19 aşısı Sputnik V uygulanan kişilerin test sonuçlarının değerlendirildiği bir makale, The Lancet tıp dergisinde yayımlandı. Bugün yayımlanan çalışmanın sonuçlarına göre, aşı uygulanan 76 kişinin tamamında antikor oluştu ve ölümcül bir yan etki tespit edilmedi. Sputnik V aşısının gönüllülerde uygulanmaya başlanacağının açıklandığı dönemde hiç bir klinik ve bilimsel araştırma sonucu açıklanmadığı için aşıya karşı çok ciddi şüpheler oluşmuştu. Sputnik-V aşısı adını, Sovyetler Birliği tarafından uzaya gönderilen ilk uydudan alıyor. Aşıya ilişkin ciddi eleştiriler ile karşı karşıya kalan Rus yetkililer ise Lancet’in yayınını memnuniyetle karşıladıklarını açıkladılar. Rusya, iki doz şeklinde uygulanan Sputnik V aşısını ağustos ayında henüz herhangi bir veri olmadan lisanslayarak faz III aşamasına geçtiğini açıklayan ilk ülke olmuştu.
Lancet dergisinde yayımlanan makalede her birinde 38 sağlıklı bireyin yer aldığı 42 günlük iki farklı testte aşı ile ilgili olumsuz hiçbir bulgu saptanmadığı ve tüm deneklerde antikor geliştiğinin tespit edildiği belirtiliyor. Ancak uzun dönem sonuçların tespiti için daha kapsamlı çalışmaların yapılması gerektiği vurgulanıyor.
Putin’in ‘ilk koronavirüs aşısı’ dediği Sputnik V hakkında neler biliniyor?
Sputnik V aşısı ile ilgili çalışma bulguları neler?
Sputnik V aşısı rekombinant adenovirüs tip 26 (rAd26) vektörü ve bir rekombinant adenovirüs tip 5 (rAd5) vektöründen oluşuyor. Araştırma kapsamında aşının iki formülünün güvenliğini ve immünojenisitesi değerlendiriliyor. Bu amaçla Rusya’daki iki hastanede iki açık, randomize olmayan faz 1/2 çalışması yapılmış. Her iki çalışmaya da 18-60 yaşları arasındaki sağlıklı yetişkinler alınıyor. Her çalışmanın 1. fazında, bir doz rAd26-S veya bir doz rAd5-S uygulandıktan 28 gün sonra güvenliği değerlendiriliyor. 18 Haziran – 3 Ağustos 2020 tarihleri arasında iki çalışmaya 76 katılımcı alınıyor.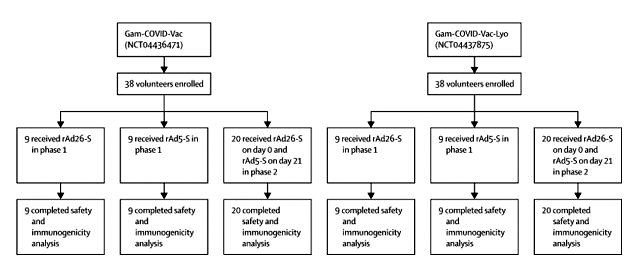 Araştırmacılar, çalışma sürecinde yaptıkları test ve gözlemlerde ciddi düzeyde bir yan etki tespit etmediklerini açıklıyorlar. Yapılan değerlendirmede tüm katılımcılarda SARS-CoV-2 glikoproteinine karşı antikor geliştiği belirtiliyor ve aşının yaygın kullanımı için daha kapsamlı çalışmalar yapılması gerektiği çağrısında bulunuluyor.
Araştırmacılar, çalışma sürecinde yaptıkları test ve gözlemlerde ciddi düzeyde bir yan etki tespit etmediklerini açıklıyorlar. Yapılan değerlendirmede tüm katılımcılarda SARS-CoV-2 glikoproteinine karşı antikor geliştiği belirtiliyor ve aşının yaygın kullanımı için daha kapsamlı çalışmalar yapılması gerektiği çağrısında bulunuluyor.
Bağımsız kurumların test sonuçları beklenmeli
Sputnik V aşısı ile ilgili yayımlanan ilk veriler memnuniyet yaratsa da, bağımsız uzmanlar yine de uluslararası standartlarda testlerin yapılması gerektiğini, bağımsız çalışmalar yayımlanmadan bu aşının kullanıma girmesinin doğru olmayacağı uyarısında bulunuyor. Öte yandan Sputnik V aşısı için sürdürülen ve uzun dönem etkilerinin tespitini amaçlayan 40 bin adet aşı uygulamasını kapsayan çalışmanın sonuçları daha doğru ve belirleyici olacaktır.
Makale Özeti
Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations: two open, non-randomised phase 1/2 studies from Russia
Background: We developed a heterologous COVID-19 vaccine consisting of two components, a recombinant adenovirus type 26 (rAd26) vector and a recombinant adenovirus type 5 (rAd5) vector, both carrying the gene for severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) spike glycoprotein (rAd26-S and rAd5-S). We aimed to assess the safety and immunogenicity of two formulations (frozen and lyophilised) of this vaccine.
Methods: We did two open, non-randomised phase 1/2 studies at two hospitals in Russia. We enrolled healthy adult volunteers (men and women) aged 18–60 years to both studies. In phase 1 of each study, we administered intramuscularly on day 0 either one dose of rAd26-S or one dose of rAd5-S and assessed the safety of the two components for 28 days. In phase 2 of the study, which began no earlier than 5 days after phase 1 vaccination, we administered intramuscularly a prime-boost vaccination, with rAd26-S given on day 0 and rAd5-S on day 21. Primary outcome measures were antigen-specific humoral immunity (SARS-CoV-2-specific antibodies measured by ELISA on days 0, 14, 21, 28, and 42) and safety (number of participants with adverse events monitored throughout the study). Secondary outcome measures were antigen-specific cellular immunity (T-cell responses and interferon-γ concentration) and change in neutralising antibodies (detected with a SARS-CoV-2 neutralisation assay). These trials are registered with ClinicalTrials.gov, NCT04436471 and NCT04437875.
Findings: Between June 18 and Aug 3, 2020, we enrolled 76 participants to the two studies (38 in each study). In each study, nine volunteers received rAd26-S in phase 1, nine received rAd5-S in phase 1, and 20 received rAd26-S and rAd5-S in phase 2. Both vaccine formulations were safe and well tolerated. The most common adverse events were pain at injection site (44 [58%]), hyperthermia (38 [50%]), headache (32 [42%]), asthenia (21 [28%]), and muscle and joint pain (18 [24%]). Most adverse events were mild and no serious adverse events were detected. All participants produced antibodies to SARS-CoV-2 glycoprotein. At day 42, receptor binding domain-specific IgG titres were 14 703 with the frozen formulation and 11 143 with the lyophilised formulation, and neutralising antibodies were 49·25 with the frozen formulation and 45·95 with the lyophilised formulation, with a seroconversion rate of 100%. Cell-mediated responses were detected in all participants at day 28, with median cell proliferation of 2·5% CD4+ and 1·3% CD8+ with the frozen formulation, and a median cell proliferation of 1·3% CD4+ and 1·1% CD8+ with the lyophilised formulation.
Interpretation: The heterologous rAd26 and rAd5 vector-based COVID-19 vaccine has a good safety profile and induced strong humoral and cellular immune responses in participants. Further investigation is needed of the effectiveness of this vaccine for prevention of COVID-19.
Funding: Ministry of Health of the Russian Federation.
Kaynaklar ve Referanslar:
1- Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations: two open, non-randomised phase 1/2 studies from RussiaYAZIYI PAYLAŞ



 Covid-19: Koronavirüs testleri, tedavisi ve aşı çalışmaları
Covid-19: Koronavirüs testleri, tedavisi ve aşı çalışmaları COVID-19 antikor testi toplum bağışıklığının belirlenmesi için çok önemli
COVID-19 antikor testi toplum bağışıklığının belirlenmesi için çok önemli Metastatik kanserlerde hedefe yönelik tedavi seçenekleri artıyor
Metastatik kanserlerde hedefe yönelik tedavi seçenekleri artıyor
YORUMUNUZ VAR MI?