Çiçek virüsü meme kanseri tedavisinde kullanılabilir mi?
 New York Memorial Sloan-Kettering Kanser Merkezi araştırmacıları, hem onkolitik hem de antianjiyojenik ajan olarak etki gösteren yeni bir çiçek hastalığı virüsü saptadılar. Amerikan Klinik Cerrahlar Derneği Kongresi’nde sunulan bulgular sayesinde, meme kanserine karşı etkili bir tedavi geliştirilebileceği öne sürüldü. Literatür verilerine göre, TNBC meme kanserinin %10-20’sinden sorumlu olan bir türüdür. TNBC, genç kadınlarda görülür (<35 yaş). TNBC’li kadınlarda östrojen, progesteron ve HER2 reseptörü olmadığı için tedavisi de güçtür. TNBC tanısı konmuş kadınlar, özellikle ileriki evrelerde, kemoterapiye başlangıçta yanıt verse de, bu tümörler genellikle daha agresiftir ve nüks etme olasılıkları yüksektir.
New York Memorial Sloan-Kettering Kanser Merkezi araştırmacıları, hem onkolitik hem de antianjiyojenik ajan olarak etki gösteren yeni bir çiçek hastalığı virüsü saptadılar. Amerikan Klinik Cerrahlar Derneği Kongresi’nde sunulan bulgular sayesinde, meme kanserine karşı etkili bir tedavi geliştirilebileceği öne sürüldü. Literatür verilerine göre, TNBC meme kanserinin %10-20’sinden sorumlu olan bir türüdür. TNBC, genç kadınlarda görülür (<35 yaş). TNBC’li kadınlarda östrojen, progesteron ve HER2 reseptörü olmadığı için tedavisi de güçtür. TNBC tanısı konmuş kadınlar, özellikle ileriki evrelerde, kemoterapiye başlangıçta yanıt verse de, bu tümörler genellikle daha agresiftir ve nüks etme olasılıkları yüksektir.
TNBC agresif karakterinin ve tedavi sonrası nüksünün henüz tam olarak açıklanamadığını hatırlatan çalışmanın baş araştırmacısı Palo Alto Standford Üniversitesi Tıp Fakültesi öğretim görevlisi Dr. Sepideh Gholami, şu bilgileri verdi: “TNBC’yi araştırmamızın bir nedeni de, bu hastalarda uzun süreli tedavi seçeneğinin az olması. Ancak bu spesifik kanser hücrelerinin benzersiz yatkınlıklarından faydalanan onkolitik virüsler inceleniyor. Çiçek hastalığı virüsünü kullanmamızın nedeni, bildiğimiz üzere, çiçek aşısının milyonlarca insanda işe yarıyor olması. Bu nedenle bu yöntemin klinik uygulamada ve gerçek hayatta güvenli ve ümit verici olacağını düşündük. Araştırmamız, TNBC’yi hedef alan yeni bir onkolitik virüsü kapsıyor ve bu spesifik yaklaşımı kullanan ve sunulan ilk araştırma niteliğinde.”
Bu çalışmada Dr. Gholami ve meslektaşları, GLV-1h164 adı verilen, vasküler endotelyal büyüme faktörünü (VEGF) hedef alan bir proteini taşıyan ve tümörün büyümesini hızlandıran anjiyogenez prosesini hızlandıran yeni bir çiçek virüsünü araştırdı. Araştırmacılar TNBC hücrelerini virüs ile enfekte etti ve TNBC hücrelerinin içindeki hücrelerin %90’ı dört gün içerisinde öldü. Daha sonra bir fare modelinde TNBC tümörü oluşturuldu. Tümörü virüs ile tedavi ettikten ve 3. haftada tümörün boyutunu ölçtükten sonra, tümörün büyük ölçüde yok edildiğini belirledi.
 Dr. Gholami, patolojiye göre tümörlerin en az %60’ının tamamen regrese olduğunu ve %40’ının da çok sayıda nekrozlu birkaç tümör hücresine sahip olduğunu tespit ettiklerini belirtti ve ekledi: “Bu, tümörün tedaviye yanıt verdiğini gösteriyor. Bu spesifik virüs, hem kanser hücrelerini enfekte edip parçalıyor, hem de tümör kan damarının büyümesini baskılıyor. Tümörü ultrasonografi ile inceledik ve yeni virüs ile tedavi edilen tümörlerin kan akışında önemli düzeyde azalma gördük. Daha da önemlisi, boyanmış tümör vaskülatürünü inceledik ve farelerin en az yarısında tümörün tedavi edildiğini saptadık. Bu bulgular, araştırmacıların klinik çalışmada TNBC hastalarına yönelik yeni virüsün güvenliliğini değerlendirecek yeni bir klinik çalışmanın tasarlanmasının da önünü açabilir.”
Dr. Gholami, patolojiye göre tümörlerin en az %60’ının tamamen regrese olduğunu ve %40’ının da çok sayıda nekrozlu birkaç tümör hücresine sahip olduğunu tespit ettiklerini belirtti ve ekledi: “Bu, tümörün tedaviye yanıt verdiğini gösteriyor. Bu spesifik virüs, hem kanser hücrelerini enfekte edip parçalıyor, hem de tümör kan damarının büyümesini baskılıyor. Tümörü ultrasonografi ile inceledik ve yeni virüs ile tedavi edilen tümörlerin kan akışında önemli düzeyde azalma gördük. Daha da önemlisi, boyanmış tümör vaskülatürünü inceledik ve farelerin en az yarısında tümörün tedavi edildiğini saptadık. Bu bulgular, araştırmacıların klinik çalışmada TNBC hastalarına yönelik yeni virüsün güvenliliğini değerlendirecek yeni bir klinik çalışmanın tasarlanmasının da önünü açabilir.”
KAYNAK: Identification of human triple-negative breast cancer subtypes and preclinical models for selection of targeted therapies. Brian D. Lehmann, Joshua A. Bauer, Xi Chen, Melinda E. Sanders, A. Bapsi Chakravarthy, Yu Shyr, Jennifer A. Pietenpol. Journal of Clinical Investigation, 2011; 121 (7): 2750 DOI: 10.1172/JCI45014
Makalenin tam metnine aşağıdaki linkten ulaşılabilmektedir:
http://www.jci.org/articles/view/45014
Abstract
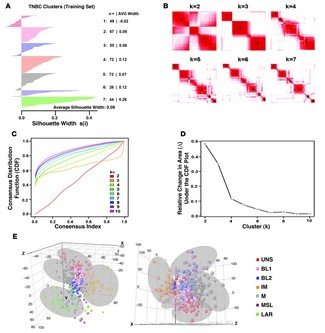 Triple-negative breast cancer (TNBC) is a highly diverse group of cancers, and subtyping is necessary to better identify molecular-based therapies. In this study, we analyzed gene expression (GE) profiles from 21 breast cancer data sets and identified 587 TNBC cases. Cluster analysis identified 6 TNBC subtypes displaying unique GE and ontologies, including 2 basal-like (BL1 and BL2), an immunomodulatory (IM), a mesenchymal (M), a mesenchymal stem–like (MSL), and a luminal androgen receptor (LAR) subtype. Further, GE analysis allowed us to identify TNBC cell line models representative of these subtypes. Predicted “driver” signaling pathways were pharmacologically targeted in these cell line models as proof of concept that analysis of distinct GE signatures can inform therapy selection. BL1 and BL2 subtypes had higher expression of cell cycle and DNA damage response genes, and representative cell lines preferentially responded to cisplatin. M and MSL subtypes were enriched in GE for epithelial-mesenchymal transition, and growth factor pathways and cell models responded to NVP-BEZ235 (a PI3K/mTOR inhibitor) and dasatinib (an abl/src inhibitor). The LAR subtype includes patients with decreased relapse-free survival and was characterized by androgen receptor (AR) signaling. LAR cell lines were uniquely sensitive to bicalutamide (an AR antagonist). These data may be useful in biomarker selection, drug discovery, and clinical trial design that will enable alignment of TNBC patients to appropriate targeted therapies.
Triple-negative breast cancer (TNBC) is a highly diverse group of cancers, and subtyping is necessary to better identify molecular-based therapies. In this study, we analyzed gene expression (GE) profiles from 21 breast cancer data sets and identified 587 TNBC cases. Cluster analysis identified 6 TNBC subtypes displaying unique GE and ontologies, including 2 basal-like (BL1 and BL2), an immunomodulatory (IM), a mesenchymal (M), a mesenchymal stem–like (MSL), and a luminal androgen receptor (LAR) subtype. Further, GE analysis allowed us to identify TNBC cell line models representative of these subtypes. Predicted “driver” signaling pathways were pharmacologically targeted in these cell line models as proof of concept that analysis of distinct GE signatures can inform therapy selection. BL1 and BL2 subtypes had higher expression of cell cycle and DNA damage response genes, and representative cell lines preferentially responded to cisplatin. M and MSL subtypes were enriched in GE for epithelial-mesenchymal transition, and growth factor pathways and cell models responded to NVP-BEZ235 (a PI3K/mTOR inhibitor) and dasatinib (an abl/src inhibitor). The LAR subtype includes patients with decreased relapse-free survival and was characterized by androgen receptor (AR) signaling. LAR cell lines were uniquely sensitive to bicalutamide (an AR antagonist). These data may be useful in biomarker selection, drug discovery, and clinical trial design that will enable alignment of TNBC patients to appropriate targeted therapies.
YAZIYI PAYLAŞ


 Kadınlarda ve erkeklerde en sık görülen kanser türleri ve tedavileri
Kadınlarda ve erkeklerde en sık görülen kanser türleri ve tedavileri Şiddetli baş ağrısı beyin tümörünün habercisi olabilir
Şiddetli baş ağrısı beyin tümörünün habercisi olabilir Nanoelmaslar meme kanseri tedavisinin etkililiğini artırabilir
Nanoelmaslar meme kanseri tedavisinin etkililiğini artırabilir Alerji nedir, kimlerde görülür? Belirtileri, testi ve tedavisi
Alerji nedir, kimlerde görülür? Belirtileri, testi ve tedavisi Meme kanserinin alt tiplerini belirmek için yeni bir markır geliyor: PAM50
Meme kanserinin alt tiplerini belirmek için yeni bir markır geliyor: PAM50
YORUMUNUZ VAR MI?