Yeni Nesil Nanoterapi İlaca Dirençli Kanser Hücrelerini Başarıyla Yok Etti!
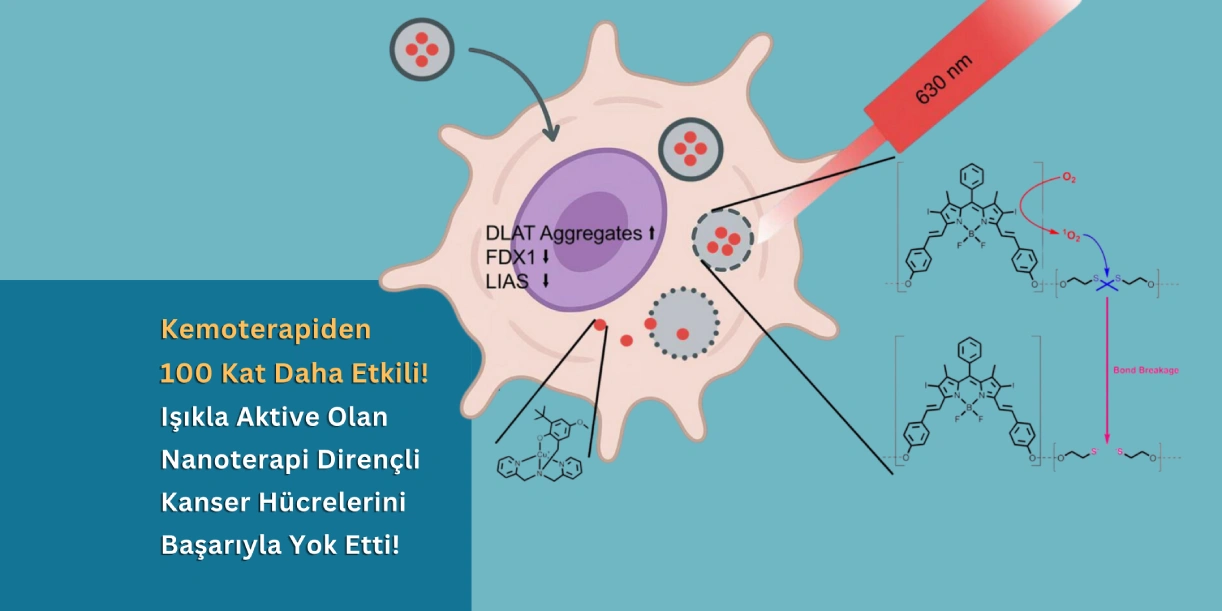
Yeni geliştirilen ve ışıkla aktive olan bakır nanopartiküller, ilaca dirençli kanserlerde cuproptosis’i tetikleyerek tümör hücrelerini hiçbir yan etkiye yol açmadan yok etti. Ruhr Üniversitesi’nden bir grup bilim insanı tarafından geliştirilen bu yeni yaklaşım, apoptoza dayalı etki eden platin bazlı kemoterapi ilaçlarından 100 kat daha güçlü bir etkiye sahip. Karanlıkta inaktif hale geçen bu parçacıklar vücuda enjekte edildiğinde doğrudan tümör hücrelerine yapışıyor. Işıkla aktive edildiklerinde kanser hücrelerini öldürüyor ve hiçbir yan etkiye neden olmadan vücuttan atılıyor.
Mevcut kanser tedavisi uzun yıllardır standart bir stratejiye dayanıyor: sitotoksik ilacı sistemik olarak vücuda vermek, yeterli miktarının tümöre ulaşmasını ummak ve bu süreçte sağlıklı dokuların da zarar görebileceğini kabul etmek. Ruhr Üniversitesi Bochum araştırmacıları tarafından geliştilen ve Advanced Functional Materials dergisinde yayımlanan yenilikçi bir çalışma ise farklı bir çözümün mümkün olabileceğini gösteriyor.
Tedavide Yeni Paradigma: İlaca Dirençli Kanserler İçin Yeni Bir Molekül Keşfedildi
Kanser tedavisinde yeni bir paradigma: cuproptosis
Bu yaklaşımın merkezinde, ilk kez 2022 yılında tanımlanan bakıra bağılı bir hücre ölüm mekanizması olan cuproptosis yer alıyor. Pek çok klasik kemoterapinin temelini oluşturan apoptozdan farklı olarak, cuproptosis tümör hücresinin metabolik çekirdeğini hedef alıyor. Araştırmacılar, karanlıkta inaktif kalan ancak kırmızı ışıkla uyarıldığında bakır temelli sitotoksik yükünü serbest bırakan ışığa duyarlı bir nanopartikül sistemi geliştirdi. Dirençli insan meme kanseri hücrelerinde test edilen bu yöntem güçlü antikanser aktivite gösterdi.
Elde edilen sonuçların önemine vurgu yapan araştırmacılar, yöntemin dirençli kanser hücrelerinde tam başarı sağladığını belirtiyor. Bu gelişme çok önemseniyor çünkü kanser hücrelerinde tedaviye karşı gelişen direnç halen kemoterapinin aşılması en zor sorunlarından biri olarak görülüyor.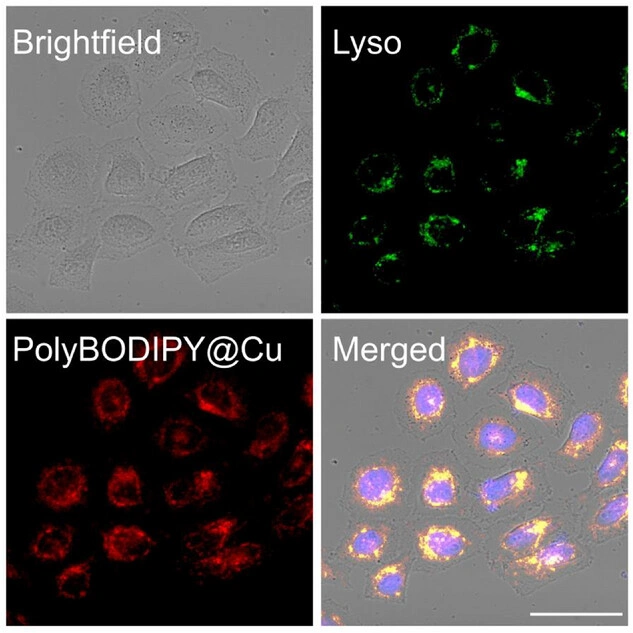
Pek çok antikanser ilaç, kanser hücrelerini öldüremediği için değil, tümörlerin bu ilaçların hedef aldığı ölüm yollarına uyum geliştirmesi nedeniyle zamanla gelişen direnç nedeniyle etkisini kaybediyor. Bochum ekibi de bu sınırlılığı, apoptoz dışı bir hücre ölüm yolunu tetikleyerek aşmayı başarmış gibi görünüyor.
Kanser hücrelerine bakır içeren nanopartüküllerle saldırı
Kanser hücreleri, değişmiş metabolik gereksinimleri nedeniyle bakırı çoğu zaman sağlıklı hücrelerden farklı şekilde işliyor. Çalışmanın yazarlarından, Ruhr Üniversitesi Bochum Tıp Fakültesi Biyofizik Bölümü’nden Prof. Dr. Johannes Karges bu durumu şöyle açıklıyor: “Bu hücre ölümü türünü bu kadar benzersiz kılan şey, hücrenin enerji üretimini hedeflemedeki özgüllüğüdür. Kanser hücreleri sıklıkla değişmiş, özellikle yoğun bir metabolizmaya sahiptir ve sağlıklı dokulara kıyasla daha fazla bakır emilimi yapar.”
Genetiği Değiştirilmiş Onkolitik Virüs Tedavisi, Cilt Kanserine Karşı Başarılı Oldu
Geliştirilen sistem birkaç kontrol katmanını bir araya getiriyor. Yapının merkezinde, aktif sitotoksik ajan olarak görev yapan tripod yapılı bir bakır-II kompleksi bulunuyor. Bu kompleks, amfifilik polimerik nanopartiküllerin içine yerleştiriliyor. Bu nanopartiküller kendi kendine birleşerek, ilacı taşıyan hidrofobik iç bölgeye ve kolloidal stabilite ile biyouyumluluğu artıran PEG fonksiyonlu dış yüzeye sahip kararlı küresel yapılar oluşturuyor. Polimer omurgasına ayrıca bir BODIPY fotosensitizörü ile reaktif oksijen türlerine duyarlı bir bağlayıcı entegre ediliyor.
Işıkla Aktive Olan Hedefli Tedavi
Normal koşullarda bu nanopartiküller, ışık uygulanmayan fizyolojik koşullarda bütünlüğünü koruyor. Kırmızı ışık uyguladığında ise BODIPY birimi singlet oksijen üretiyor, bu da bağlayıcıyı oksitleyerek nanopartikülün dağılmasına neden oluyor. Böylece bakır kompleksi sistemik olarak değil, lokal olarak serbest bırakılıyor.
Prof. Dr. Karges mekanizmanın işleyişini şöyle özetliyor: “Salım ilkesi, temel polimer iskelet içindeki ışığa duyarlı bir bağa dayanıyor. Işık uygulaması bu özel bağı seçici olarak koparıyor, bunun ardından nanopartiküller çözünüyor ve bakır kompleksi lokal olarak serbest kalıyor.”
Pankreas Kanseri Tedavisinde Yeni Umut: ADC Teknolojisiyle Geliştirilen İlaç Yolda
Bu tasarım, platforma hem mekânsal hem de zamansal hassasiyet kazandırıyor. Parçacıkların vücuda enjekte edildiğinde özellikle tümör dokusunda birikiyor ve polimer kılıf erken salımı önlemeye yardımcı oluyor. Tedavi edici etki ancak hedefe yönelik ışık uygulamasından sonra devreye giriyor. İlke olarak bu durum, standart kemoterapinin başlıca zayıf yönlerinden biri olan hedef dışı toksisiteyi azaltıyor.
Mekanistik açıdan bakıldığında, salınan bakır kompleksi cuproptosis’i, lipoik asit sentetaz ile mitokondriyal metabolizmanın düzenleyicilerini bozarak tetikliyor. Sonuçta ciddi proteotoksik ve metabolik stres gelişiyor ve bu da, platin bazlı ilaçların yaygın olarak kullandığı yollardan farklı bir mekanizma üzerinden hücre ölümüne yol açıyor.
Mevcut kemoterapilerden 100 kat daha etkili
Yazarların bildirdiğine göre bu platform, deneysel koşullarda klinikte kullanılan platin türevlerinden yaklaşık 100 kat daha etkili bulundu. En az bunun kadar önemli bir diğer nokta da aktivitenin çoklu ilaca dirençli kanser hücresi türevlerinde de korunmuş olması.
Tek Dozla Meme Kanseri Tümörlerini Yok Edebilen Yeni İlaç Adayı
Yeni yöntemin klasik kanser ilaçlarının etkisini azaltan direnç mekanizmalarını aşabildiğini söyleyen Prof. Dr. Karges, hedefleri ile şu bilgileri paylaştı: “Bu yöntemin, klasik kemoterapi tedavilerinin sınırlarına ulaştığı tedaviye dirençli kanser hücrelerinde çok etkili olduğunu gösterebildik. Bu yöntemin başarısını laboratuvarda dirençli kanser hücrelerinde gösterdik. Şimdiki hedefimiz ise en kısa sürede bu yönetimi klinik ortamda kanser hastalarında test etmek.”
Kaynaklar ve Referanslar:
1- Light Activated Induction of Cuproptosis in Resistant Cancer Cells Using Polymeric BODIPY Nanoparticles for Photoactivated Chemotherapy2- Light-Activated Copper Nanoparticles Trigger Cuproptosis in Drug-Resistant Cancer CellsYAZIYI PAYLAŞ



 Kadınlarda ve erkeklerde en sık görülen kanser türleri ve tedavileri
Kadınlarda ve erkeklerde en sık görülen kanser türleri ve tedavileri Çocuk gelişimi ve psikolojisi: Gelişimini etkileyen faktörler
Çocuk gelişimi ve psikolojisi: Gelişimini etkileyen faktörler Tedavide Yeni Paradigma: İlaca Dirençli Kanserler İçin Yeni Bir Molekül Keşfedildi
Tedavide Yeni Paradigma: İlaca Dirençli Kanserler İçin Yeni Bir Molekül Keşfedildi Yapay Zekâ ile Tasarlanan Proteinler, Kanser Hücrelerini Hedef Haline Getirip Yok Ediyor
Yapay Zekâ ile Tasarlanan Proteinler, Kanser Hücrelerini Hedef Haline Getirip Yok Ediyor İmmünoterapi nedir, nasıl uygulanır? Kanser tedavisindeki faydaları
İmmünoterapi nedir, nasıl uygulanır? Kanser tedavisindeki faydaları
YORUMUNUZ VAR MI?