Kanser ve Genetik Hastalıkların Tedavisinde Yeni Dönem: Nanopartiküller ile Gen Transferi

Michigan Üniversitesi araştırmacıları, viral vektör kullanmadan plazmid DNA ve mRNA’yı farklı insan hücre tiplerine taşıyabilen serum albümini bazlı nanopartiküller geliştirdi. Advanced Materials dergisinde yayımlanan çalışmada, bu platform ile üretilen nanopartiküllerin hücreler tarafından %95 oranında absorbe edildi. Ayrıca 12 gün boyunca kararlı kaldı ve primer insan T hücrelerinde yüksek canlılık korunarak etkili transfeksiyon sağlandı. Araştırmacılara göre bu yaklaşım, viral taşıyıcılara bağlı riskleri azaltarak kanser ve birçok genetik hastalık için daha güvenli gen tedavilerinin önünü açabilir.
Gen terapileri başta kan hastalıkları olmak üzere pek çok kanser türünün tedavisinde önemli bir dönüşüm yaratmaya başlamış durumda. Geçtiğimiz birkaç yıl içerisinde bu alandaki viral bazlı bazı tedaviler onaylanarak kullanıma girdi. Ancak genlerin hücrelere ulaştırılmasında kullanılan sistemler halen ciddi sınırlılıklar barındırıyor. Mevcut onaylı yöntemler terapötik genleri hücre içine taşımak için modifiye virüslerden yararlanılıyor. Bu strateji oldukça etkili olsa da ciddi riskleri de barındırıyor. Aşırı bağışıklık yanıtları, inflamatuvar toksisite ve viral materyalin genoma entegre olarak tümör baskılayıcı genleri bozması ve ikincil kanserlere neden olması, bu risklerden sadece bir kaçı.
mRNA teknolojisi tıpta oyunun kurallarını değiştiriyor: Kanser karşı çare olabilir!
Daha Güvenli Bir Taşıma Stratejisi
Michigan Üniversitesi Mühendislik Fakültesi ile Michigan Medicine’den bir ekip, bu soruna farklı bir çözüm geliştirmeyi başardı. Araştırmacılar, protein nanopartiküllerinden oluşan nonviral bir taşıma platformunu geliştirdiler. Bu sistem, genetik materyali karaciğer kanseri hücreleri, böbrek hücreleri ve primer insan T hücreleri dahil olmak üzere çeşitli insan hücre tiplerine başarıyla ulaştırabiliyor. Çalışmanın bulguları, yeni yöntemin özellikle genom bütünlüğünün korunmasının kritik olduğu durumlarda, gen transferi için daha güvenli bir çerçeve sunabileceğine işaret ediyor.
Partiküller Nasıl Kararlı Hale Getiriliyor?
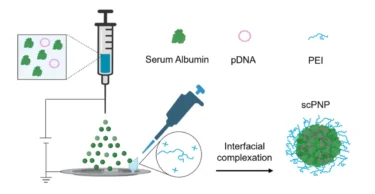
scPNP sentezi ve karakterizasyonu ve scPNP üretim şeması: Yüzey kaplama öncesi protein nanopartiküllerinin SEM görüntüsü ve çap ölçümleri verildi. PEI ile kaplama sonrası, silikon çip üzerine bırakılan partiküllerin SEM görüntüsü ve çap analizi sunuldu. Veriler, 5 farklı görüntüdeki tekil partiküllerden elde edildi. DLS analizinde scPNP’lerin hidrodinamik çap dağılımı sayı bazlı ve yoğunluk bazlı olarak gösterildi. Su içinde toplanan partiküllerin parçalandığı görüldü ve bu bulgu, polikatyonun arayüzey kompleksleşmesiyle sağlanan stabilizasyonun önemini ortaya koymaktadır.
Platformun yapısal çekirdeğini, kanda doğal olarak bulunan bir protein olan serum albümini oluşturuyor. DNA veya haberci RNA, bu çekirdeğin içine kapsülleniyor. Partikül yüzeyi ise kimyasal çapraz bağlama yerine arayüzey kompleksleşmesi yoluyla polikatyonik bir polimerle kaplanıyor. Bu tasarım sayesinde partiküller fizyolojik pH koşullarında 12 güne kadar kararlı kalabiliyor. Ayrıca ağırlıkça %10 ila %40 arasında değişen, alışılmadık derecede yoğun nükleik asit yükleri taşıyabiliyor. Çalışmaya göre bu, partikül başına yaklaşık 28 ila 99 plazmide karşılık geliyor.
Biyolojide devrim! CRISPR/Co9 teknolojisi ile cilt hücreleri kök hücreye dönüştürüldü
Hücre deneylerinde nanopartiküller, yeşil floresan proteini kodlayan genleri taşımak için kullanıldı. İnsan karaciğer kanseri hücreleri, böbrek hücreleri ve bağışıklık hücreleri, partikülleri alıp genetik yükü işledikten sonra yeşil ışık yaymaya başladı. Bu da taşınan genetik materyalin başarıyla serbest bırakıldığını ve eksprese edildiğini kanıtlıyor.
Çalışmanın sorumlu yazarı, Michigan Üniversitesi Biointerfaces Institute Direktörü ve Kimya Mühendisliği Profesörü Joerg Lahann, konuya ilişkin şu değerlendirmeyi yaptı: “Tek bir mutasyon nedeniyle bir proteinin eksik olduğu ya da işlevini kaybettiği çok sayıda hastalık var ve yeni bir gen vererek bunu kesinlikle düzeltebiliriz. Genellikle bu işlem virüslerle yapılıyor, ancak virüsler toksik olabilir ve bağışıklık hücrelerini aşırı aktive edebilir. Bu nedenle alanda, virüs temelli gen düzenleme stratejilerinin yerini alabilecek yaklaşımlara yönelik güçlü bir ihtiyaç var.”
Partiküller Nasıl Üretiliyor?
Nanopartiküller, elektrohidrodinamik jetleme adı verilen bir yöntemle üretiliyor. Bu yöntemde protein ve nükleik asit karışımı bir elektrik alan içinden hızlandırılıyor. Su hızla buharlaşırken protein, taşınan genetik yükün etrafında yoğunlaşıyor. Hücreler partikülleri içine aldıktan sonra bunlar endozomlara giriyor. Burada pozitif yüklü yüzey polimerinin osmotik bir dengesizlik oluşturduğu, suyu içeri çekerek endozomun parçalanmasına ve yükün hücre içine salınmasına yol açıyor.
Yeni Nesil Nanoterapi İlaca Dirençli Kanser Hücrelerini Başarıyla Yok Etti!
Mekanik açıdan test edildiğinde sistemin güçlü bir performans gösterdiği saptandı. Hücreler tarafından alım verimi yüzde 95’in üzerine çıktı ve partiküllerin hücre içine hem makropinositoz hem de klatrin aracılı endositoz yoluyla girdiği görüldü. Çalışma ayrıca önemli bir optimizasyon ilkesini de ortaya koydu. Toplam plazmid miktarı sabit tutulduğunda, yük yoğunluğunu artırmak yerine nanopartikül dozunu artırmak daha etkili oldu ve transfeksiyon oranında 1,6 kat iyileşme sağladı.
Bu bulgu, verimlilik, canlılık ve tekrarlanabilirliğin büyük önem taşıdığı hücre tedavisi üretim süreçleri açısından devrim niteliğinde sonuçlar doğurabilir. Özellikle primer insan T hücrelerinden elde edilen sonuçlar dikkat çekiciydi. Çünkü bu hücreler, nonviral taşıma sistemleri açısından zor hedefler arasında yer alıyor. Araştırmacılar, bu hücrelerde yüksek canlılığı korurken etkili mRNA transfeksiyonu sağlandığını ve sistemin bu koşullarda Lipofectamine MessengerMax’tan daha iyi performans gösterdiğini bildirdiler.
Güvenlik ile Kalıcılık Arasındaki Denge
Bu yaklaşımın güvenlik mantığı oldukça net. Taşınan plazmid DNA veya mRNA, konak genomuna entegre olmadığından, entegre olabilen viral vektörlerin bazen yaptığı gibi doğal genleri bozması beklenmiyor. Ancak bunun bir karşılığı var: kalıcılık daha sınırlı. mRNA yalnızca birkaç gün boyunca varlığını sürdürüyor, plazmid DNA ise en fazla birkaç ay kalabiliyor. Bu nedenle bazı uygulamalarda tekrarlayan dozlar gerekebiliyor.
Mayo Clinic’ten İleri Evre Kanserlere Karşı Nanopartikül Hipertermi Tedavisi!
Diğer bazı kullanım alanlarında ise bu platform, geçici ama daha güvenli bir taşıma aracı olarak değerlendirilebilir. Yazarlar ayrıca, nanopartiküllerin ileride CRISPR-Cas9 bileşenleriyle yüklenmesinin, daha hassas ve daha kalıcı gen düzeltmelerine imkan sağlayabileceğini de belirtiyor.
Platformun siRNA, antisens oligonükleotidler veya Cas9-sgRNA komplekslerine uyarlanması da teorik olarak mümkün görünüyor. Ayrıca protein kabuğu değiştirilerek partiküllerin belirli hücre tiplerine daha seçici biçimde yönlendirilmesi sağlanabiliyor.
Şimdilik bu çalışma preklinik aşamada ancak gen tedavisinin en kalıcı mühendislik sorunlarından birisine çok etkili bir çözüm sunuyor. Büyük nükleik asit yükleri, viral vektörlerin biyolojik bedelini ödemeden nasıl verimli biçimde hücreye taşınabilir? Bu platform terapötik modellerde de başarılı olursa, gen ve hücre tedavilerinin virüsler, elektroporasyon ve daha sert taşıma yöntemlerinin sınırlamalarını aşarak daha geniş bir kullanım alanına ulaşmasını sağlayabilir. Böylece genetik terapi yöntemleri pek çok ölümcül hastalığın tedavisinde kesin şifa yöntemine dönüşebilir.
Kaynaklar ve Referanslar:
1- Nonviral Gene Delivery Platform Offers Promise for Cancer Treatment and Cell Therapy2- Surface-Capped Protein Nanoparticles for Nonviral Gene DeliveryYAZIYI PAYLAŞ


 mRNA teknolojisi tıpta oyunun kurallarını değiştiriyor: Kanser karşı çare olabilir!
mRNA teknolojisi tıpta oyunun kurallarını değiştiriyor: Kanser karşı çare olabilir! Çocuk gelişimi ve psikolojisi: Gelişimini etkileyen faktörler
Çocuk gelişimi ve psikolojisi: Gelişimini etkileyen faktörler Genetik mRNA teknolojisi Covid-19 dışındaki hastalıkların tedavisinde çığır açabilir
Genetik mRNA teknolojisi Covid-19 dışındaki hastalıkların tedavisinde çığır açabilir Bilimsel veriler ışığında Biontech / Pfizer ve Sinovac aşılarının yan etkileri
Bilimsel veriler ışığında Biontech / Pfizer ve Sinovac aşılarının yan etkileri Depresyon ve genetik: Mutsuzluk ve intihara neden olan genler
Depresyon ve genetik: Mutsuzluk ve intihara neden olan genler
YORUMUNUZ VAR MI?