Kanserde radyoterapinin etkisi iki katına çıkarabilir
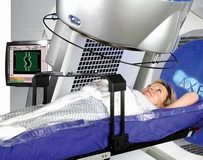 Journal of Radiation Oncology’de yayımlanan bir çalışmada kanser tedavisinde radyasyon terapisinin etkinliğinin iki katına çıkarılabileceği ve yan etkilerinin azaltılabileceği gösterildi. Georgia Sağlık Bilimleri Üniversitesi araştırmacıları akciğer kanseri hücrelerinin radyasyon tedavisinin neden olduğu letal çift sarmal DNA kırılmasını tamir etme yeteneğini azaltacak yeni bir yol buldular.
Journal of Radiation Oncology’de yayımlanan bir çalışmada kanser tedavisinde radyasyon terapisinin etkinliğinin iki katına çıkarılabileceği ve yan etkilerinin azaltılabileceği gösterildi. Georgia Sağlık Bilimleri Üniversitesi araştırmacıları akciğer kanseri hücrelerinin radyasyon tedavisinin neden olduğu letal çift sarmal DNA kırılmasını tamir etme yeteneğini azaltacak yeni bir yol buldular.
GHSU Moleküler Tıp ve Genetik Enstitüsü Nanotıp ve Gen Düzenleme Şefi ve Araştırmanın Direktör Yardımcısı Prof. Dr. William S. Dynan, “Radyasyon terapisi mükemmel bir tedavi ancak sorun ciddi yan etkilerinin olması. Yeni geliştirilen yöntemle daha az radyasyon kullanarak aynı miktarda kanser hücresini öldürmek veya aynı miktarda radyasyon kullanarak daha önce iyileştirilemeyen bir hastayı iyileştirmek mümkün olabilir. Burada önemli olan doğru hedeflerin belirlenerek terapinin o hedeflere odaklanmasıdır” dedi.
Radyasyon tedavisi, radyasyonun DNA’da çift sarmal kırılmalara neden olarak, hücre öldürme yeteneğinden yararlanır. Ancak çeşitli düzeyde radyasyon aslında her yerde bulunuyor – yiyecekler, hava, yer vs. – yani kanser hücreleri de dahil olmak üzere tüm hücreler, letal kırılmayı önleyecek iç mekanizmalara sahip. GHSU bilim insanları, bir miktar antikoru pek çok hücreye özellikle kanser hücrelerine kolaylıkla giren folat ile paketleyerek, doğal savunma mekanizmalarını hedefliyor. Çalıştıkları akciğer kanseri de dahil olmak üzere pek çok kanser çok sayıda folat reseptörüne sahip, dolayısıyla kanser hücreleri orantısız olarak bu paketleri paylaşıyorlar.
International Journal of Radiation Oncology sorumlu yazarı moleküler biyolog Prof. Dr. Shuyi Li, “Kanser hücrelerinin radyasyonun hasarını bertaraf etmesini yok etmek için gösterilen daha önceki çabalar yüzeylerindeki reseptörlere odaklanmıştı. Ancak yeni yöntem tamamen başka bir alana odaklanmış durumda” dedi.
Daha fazla direkt vuruş için bilim insanları giriş noktası olarak ScFv 18-2 antikoruyla folatı kimyasal olarak bağlayarak folat reseptörlerinin avantajını kullandılar. Paket başları hücre çekirdeği için düzdü. Hücre çekirdeğinde farklı bir kimyasal çevre, DNA tamirinde elzem bir enzim olan DNA bağıntılı protein kinazın düzenleyici bölgesine saldırmak için, ScFv 18-2’yi serbest bırakarak bağını kopartmaktadır.
 Prof. Dr. Dynan, “Hedef bir molekülü bir yük ile bağlıyoruz. Bu strateji anahtar enzimlerden birini hedeflemektedir, böylece tamiri daha zor olmaktadır. Bu durum kanser hücrelerini radyasyona karşı daha hassas kılmaktadır. Bu yaklaşım herhangi bir sayıdaki ilacı direkt olarak kanser hücrelerine ulaştırmak için de kullanılabilir. Gelecekteki çalışmalar, diğer hücre giriş noktalarını aramayı olduğu kadar en etkili pakete sahip diğer hedefleri de kapsayacak. Bugüne kadar yapılan çalışmalar insan akciğer kanseri hücre kültürlerinde gerçekleştirildi. Dolayısıyla bir sonraki aşamanın hayvan çalışmalarını da kapsaması gerekiyor” dedi.
Prof. Dr. Dynan, “Hedef bir molekülü bir yük ile bağlıyoruz. Bu strateji anahtar enzimlerden birini hedeflemektedir, böylece tamiri daha zor olmaktadır. Bu durum kanser hücrelerini radyasyona karşı daha hassas kılmaktadır. Bu yaklaşım herhangi bir sayıdaki ilacı direkt olarak kanser hücrelerine ulaştırmak için de kullanılabilir. Gelecekteki çalışmalar, diğer hücre giriş noktalarını aramayı olduğu kadar en etkili pakete sahip diğer hedefleri de kapsayacak. Bugüne kadar yapılan çalışmalar insan akciğer kanseri hücre kültürlerinde gerçekleştirildi. Dolayısıyla bir sonraki aşamanın hayvan çalışmalarını da kapsaması gerekiyor” dedi.
Yaklaşımları endositoz adı verilen doğal bir süreci taklit etmektedir. Endositozda, hücreler proteinleri ve diğer maddeleri yutar, içine girmek ister fakat normal girişe uymazlar. Folat reseptörleri, ovaryum kanseri için yeni bir stratejinin klinik çalışmasının da dahil olduğu, kemoterapötik ilaçlar için direkt giriş noktası olarak halihazırda kullanılmaktadır. GHSU, en ölümcül kanserlerden birinin daha iyi hedef olabilmesi için, kan yoluyla verilmesi çok toksik olan bir ajanı folat ile eşleştiren bir klinik çalışmayı da yürütüyor.
KAYNAK: Intranuclear Delivery of a Novel Antibody-Derived Radiosensitizer Targeting the DNA-Dependent Protein Kinase Catalytic Subunit. International Journal of Radiation Oncology. William S. Dynan, Shuyi Li. Georgia Health Sciences University.
http://www.redjournal.org/article/S0360-3016(11)03203-2/abstract
YAZIYI PAYLAŞ



 Radyasyon çalışanlarının icap nöbetleri çalışma süresinden düşülecek
Radyasyon çalışanlarının icap nöbetleri çalışma süresinden düşülecek Radyoterapi ve akıllı ilaçların birlikte kullanımı kanserde başarıyı arttıracak!
Radyoterapi ve akıllı ilaçların birlikte kullanımı kanserde başarıyı arttıracak! Kadınlarda ve erkeklerde en sık görülen kanser türleri ve tedavileri
Kadınlarda ve erkeklerde en sık görülen kanser türleri ve tedavileri Lokal ileri meme kanserinde, radyoterapinin rolü ve tedavi alanlarının seçimi
Lokal ileri meme kanserinde, radyoterapinin rolü ve tedavi alanlarının seçimi Prostat kanserinin erken teşhisi nasıl yapılır? Tedavisinde hangi yöntem etkilidir?
Prostat kanserinin erken teşhisi nasıl yapılır? Tedavisinde hangi yöntem etkilidir?
YORUMUNUZ VAR MI?